Les protéines sont de grandes biomolécules et macromolécules qui comprennent une ou plusieurs longues chaînes de résidus d'acides aminés. Mais saviez-vous que PARP-1, un type de protéine, répare constamment notre ADN endommagé ?
La PARP-1 est une protéine présente dans nos cellules qui répare constamment l'ADN endommagé. Cependant, il ne peut pas réparer l'ADN dans les neurones pendant que nous sommes éveillés. En conséquence, il s'accumule jusqu'à ce que nous nous endormions. Selon de nouvelles recherches, l'accumulation de PARP-1 nous fait dormir
Qu'est-ce que la protéine PARP-1 et où se produit la majeure partie de son activité ?
PARP-1, également connue sous le nom de NAD+ ADP-ribosyltransférase 1 ou poly ADP-ribose synthase 1, est une enzyme codée par le gène PARP1 chez l'homme. C'est la plus abondante de la famille d'enzymes PARP, représentant 90 % du NAD+ utilisé par la famille.
La PARP-1 se retrouve à la place de l'histone H1 dans les gènes actifs. Il se trouve dans le noyau cellulaire et peut détecter et répondre immédiatement aux effets métaboliques et chimiques au niveau cellulaire. (La source: Royal Society of Chemistry)
Comment la protéine PARP-1 améliore-t-elle la réparation de l'ADN dans les neurones en favorisant le sommeil ?
Les caractéristiques des moteurs du sommeil et les mécanismes par lesquels le sommeil soulage la pression de l'homéostasie cellulaire sont inconnus. Les niveaux de dommages à l'ADN chez les mouches, les poissons zèbres, les souris et les humains augmentent pendant l'éveil et diminuent pendant le sommeil. Nous montrons que 6 heures de sommeil consolidé suffisent à réduire les dommages à l'ADN dans le pallium dorsal du poisson zèbre.
Le sommeil et la réparation de l'ADN ont été déclenchés par l'induction de dommages à l'ADN par l'activité neuronale et les mutagènes. Les protéines de réponse aux dommages de l'ADN (DDR) Rad52 et Ku80 ont augmenté pendant le sommeil et la dynamique des chromosomes a augmenté l'activité de Rad52.
Suite à la privation de sommeil, l'activité de l'initiateur DDR PARP-1 a augmenté. PARP-1 a favorisé le sommeil chez les larves de poisson zèbre et les souris adultes. Son inhibition a réduit la dynamique et la réparation des chromosomes dépendant du sommeil.
Ces résultats montrent que les dommages à l'ADN sont un moteur homéostatique du sommeil et que les voies PARP-1 peuvent détecter cette pression cellulaire et faciliter le sommeil et l'activité de réparation. (La source: X-MOL)
Comment l'ADN PARP-1 détecte-t-il les cellules endommagées et réparatrices ?
En formant la modification post-traductionnelle poly ADP-ribose, PARP-1 affecte la transcription des gènes, la signalisation de la mort cellulaire et la réparation de l'ADN ADP-ribose. PARP-1 est rapidement associé à des dommages à l'ADN lors de la réponse physiologique au stress génotoxique, entraînant une puissante stimulation de la synthèse de poly ADP-ribose sur un faible niveau basal d'activité de PARP-1.
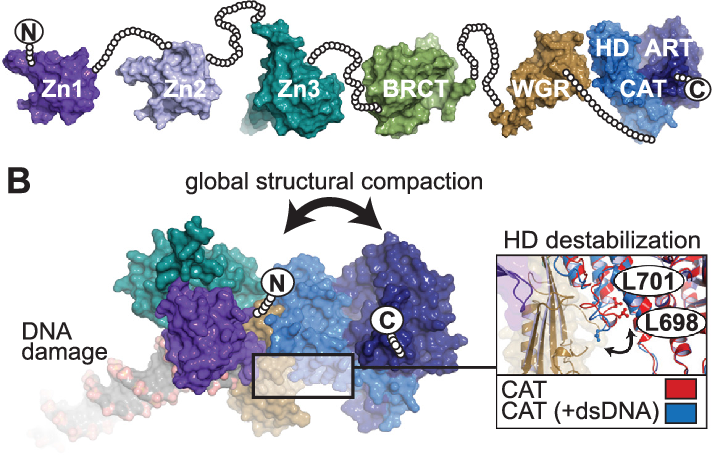
Comprendre la fonction biologique de PARP-1 dépend des dommages à l'ADN. Pourtant, les informations structurelles sur les mécanismes à l'origine de ce mode de régulation sont restées insaisissables, en partie à cause de l'architecture extrêmement modulaire à six domaines de PARP-1. PARP-1 utilise des doigts de zinc uniques pour détecter les ruptures d'ADN par le biais d'interactions indépendantes de la séquence avec des bases nucléotidiques exposées, une caractéristique typique des structures d'ADN endommagées et aberrantes, selon de récentes enquêtes structurelles.
Sur la base d'une structure cristalline des domaines critiques de PARP-1 en association avec une rupture de brin d'ADN, la méthode de connexion de la détection des dommages à l'ADN à la production améliorée de poly ADP-ribose a été révélée. Les nombreux domaines de PARP-1 entrent en collision avec l'ADN endommagé, générant un réseau d'interactions interdomaines qui provoquent des changements déstabilisants dans le domaine catalytique, entraînant une synthèse accrue de poly ADP-ribose. (La source: National Library of Medicine)