البروتينات هي جزيئات حيوية وكبيرة تتكون من سلسلة أو أكثر طويلة من بقايا الأحماض الأمينية. لكن هل تعلم أن PARP-1، وهو نوع من البروتينات، يقوم باستمرار بإصلاح الحمض النووي المتضرر لدينا؟
إن الـPARP-1 هو بروتين موجود في خلايانا يقوم باستمرار بإصلاح الحمض النووي المتضرر. ومع ذلك، لا يستطيع إصلاح الحمض النووي في الخلايا العصبية أثناء استيقاظنا. ونتيجة لذلك، يتراكم حتى نغفو. وفقًا لأبحاث جديدة، فإن تراكم الـPARP-1 يجعلنا ننام.
ما هو بروتين PARP-1، وأين يحدث معظم نشاطه؟
PARP-1، المعروف أيضًا باسم NAD+ ADP-ribosyltransferase 1 أو poly ADP-ribose synthase 1، هو إنزيم يُشفّر بواسطة جين PARP1 في البشر. وهو الأكثر وفرةً بين عائلة إنزيمات PARP، حيث يُمثل 90٪ من NAD+ المستهلكة من قبل العائلة.
يُوجد الـPARP-1 في مكان الهيستون H1 في الجينات النشطة. يتواجد في نواة الخلية ويمكنه اكتشاف والاستجابة للعمليات الأيضية والكيميائية على المستوى الخلوي فورًا. (المصدر: Royal Society of Chemistry)
كيف يُحسّن بروتين PARP-1 إصلاح الحمض النووي في الخلايا العصبية من خلال تعزيز النوم؟
خصائص محفّزات النوم والآليات التي يخفّف بها النوم ضغط التوازن الخلوي غير معروفة. مستويات تلف الحمض النووي في الذباب، وأسماك الزرد، والفئران، والبشر تزداد أثناء اليقظة وتقل أثناء النوم. نُظهر أن 6 ساعات من النوم المتواصل كافية لتقليل تلف الحمض النووي في القشرة الظهرية لأسماك الزرد.
تم تحفيز النوم وإصلاح الحمض النووي بواسطة إحداث تلف الحمض النووي نتيجة النشاط العصبي والمواد الم mutagenic. ارتفعت بروتينات استجابة تلف الحمض النووي (DDR) Rad52 وKu80 أثناء النوم، وزادت ديناميكيات الكروموسومات من نشاط Rad52.
بعد الحرمان من النوم، ارتفع نشاط مُبادِر DDR وهو PARP-1. عزّز الـPARP-1 النوم في كل من يرقات أسماك الزرد والفئران البالغة. أدى تثبيطه إلى تقليل الديناميكيات الكروموسومية المعتمدة على النوم والإصلاح.
تُظهر هذه النتائج أن تلف الحمض النووي هو محرك توازن للنعاس، وأن مسارات الـPARP-1 يمكنها اكتشاف هذا الضغط الخلوي وتسهيل النوم ونشاط الإصلاح. (المصدر: X-MOL)
كيف يكتشف الـPARP-1 تلف الحمض النووي ويُصلح الخلايا؟
من خلال تكوين التعديل ما بعد الترجمة بولي ADP-ريبوز، يؤثر الـPARP-1 على نسخ الجينات، وإشارات موت الخلية، وإصلاح الحمض النووي عبر ADP-ريبوز. يرتبط الـPARP-1 بسرعة بتلف الحمض النووي أثناء الاستجابة الفسيولوجية للضغط الجيني السام، مما يؤدي إلى تنشيط قوي لتصنيع بولي ADP-ريبوز فوق مستوى نشاط أساسي منخفض للـPARP-1.
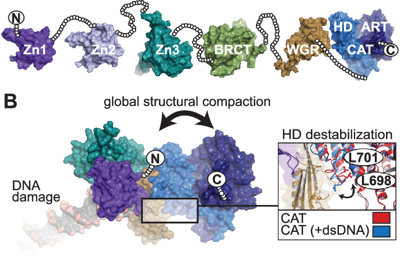
فهم الوظيفة البيولوجية لـ PARP-1 يعتمد على ضرر الحمض النووي. ومع ذلك، لا تزال الرؤى الهيكلية حول الآليات التي تكمن وراء هذا النوع من التنظيم غير واضحة، جزئياً بسبب بنية PARP-1 المكوّنة من ستة مجالات ذات طابع معياري شديد. يستخدم PARP-1 أصابع الزنك الفريدة لاكتشاف انقطاعات الحمض النووي من خلال تفاعلات مستقلة عن التسلسل مع القواعد النيوكليوتيدية المكشوفة، وهو علامة نموذجية للحمض النووي المتضرر وغير الطبيعي، وفقًا للتحقيقات الهيكلية الحديثة.
استنادًا إلى بنية بلورية للمجالات الحرجة لـ PARP-1 بالتزامن مع انقطاع شريط الحمض النووي، تم الكشف عن طريقة ربط اكتشاف ضرر الحمض النووي بزيادة إنتاج بولي ADP-ريبوز. تتصادم العديد من مجالات PARP-1 مع الحمض النووي المتضرر، مما يولد شبكة من التفاعلات بين المجالات التي تسبب تغييرات مزعزلة في المجال التحفيزي، مما يؤدي إلى زيادة تخليق بولي ADP-ريبوز. (المصدر: المكتبة الوطنية للطب)